| Лейкоцитарный антиген человека | |
|---|---|
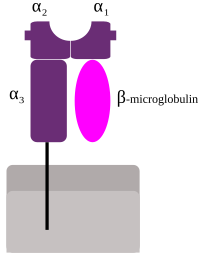 Схематическое изображение MHC класса I | |
| Идентификаторы | |
| Символ | HLA |
| ИнтерПро | IPR037055 |
| Мембранома | 63 |
Человеческого лейкоцитарного антигена ( HLA ) система или комплекс представляет собой группу родственных белков, которые кодируются с помощью главного комплекса гистосовместимости (МНС) комплекс генов в организме человека. [1] Эти белки клеточной поверхности отвечают за регуляцию иммунной системы . Генный комплекс HLA находится на участке длиной 3 Мбп в хромосоме 6p 21. Гены HLA очень полиморфны , что означает, что у них много разных аллелей , что позволяет им точно настраивать адаптивную иммунную систему . Белки, кодируемые определенными генами, также известны какантигенов в результате их исторического открытия в качестве факторов при трансплантации органов. У разных классов разные функции:
HLA, соответствующие MHC класса I ( A , B и C ), все из которых являются группой HLA Class1, представляют пептиды изнутри клетки. Например, если клетка инфицирована вирусом, система HLA переносит фрагменты вируса на поверхность клетки, чтобы клетка могла быть уничтожена иммунной системой. Эти пептиды производятся из переваренных белков, которые расщепляются в протеасомах . Как правило, эти конкретные пептиды представляют собой небольшие полимеры длиной около 8-10 аминокислот . [2] Чужеродные антигены, представленные MHC класса I, привлекают Т-лимфоциты, называемые Т-киллерами (также называемыеCD8- положительные или цитотоксические Т-клетки), разрушающие клетки. В некоторых новых работах было высказано предположение, что антигены длиной более 10 аминокислот, 11-14 аминокислот могут быть представлены на MHC I, вызывая цитотоксический Т-клеточный ответ. [3] Белки MHC класса I связаны с β2-микроглобулином , который, в отличие от белков HLA, кодируется геном на 15 хромосоме .
HLA, соответствующие MHC класса II ( DP , DM , DO , DQ и DR ), представляют антигены извне клетки Т-лимфоцитам. Эти специфические антигены стимулируют размножение Т-клеток - хелперов (называемые также CD4 - положительные Т - клетки), которые , в свою очередь , стимулируют антитела -продуцирующих В-клетки вырабатывать антитела к этому конкретному антигену. Самоантигены подавляются регуляторными Т-клетками .
HLA, соответствующие классу III MHC, кодируют компоненты системы комплемента .
У HLA есть и другие роли. Они важны для защиты от болезней. Они являются основной причиной отторжения трансплантата органов . Они могут защищать или не защищать (если их подавляет инфекция) от рака. [4] Мутации в HLA могут быть связаны с аутоиммунным заболеванием (примеры: диабет I типа , целиакия ). HLA также может быть связан с восприятием людьми запаха других людей и может быть задействован в выборе партнера, поскольку по крайней мере одно исследование показало более низкий, чем ожидалось, уровень сходства HLA между супругами в изолированном сообществе. [5]
Помимо генов, кодирующих шесть основных антигенпредставляющих белков, существует множество других генов, многие из которых участвуют в иммунной функции, расположенных в комплексе HLA. Разнообразие HLA в человеческой популяции является одним из аспектов защиты от болезней, и, как следствие, вероятность того, что у двух неродственных людей будут одинаковые молекулы HLA во всех локусах , чрезвычайно мала. Гены HLA исторически были идентифицированы в результате способности успешно трансплантировать органы между HLA-подобными людьми. [ необходима цитата ]
Функции [ править ]
Эти белки , кодируемые Hlas являются те , на внешней части клеток тела, которые (в сущности) , уникальных для этого человека. Иммунная система использует HLAs к дифференцировке клеток самостоятельно и чужеродными клетками. Любая ячейка, отображающая тип HLA этого человека, принадлежит этому человеку и, следовательно, не является захватчиком.
При инфекционных заболеваниях [ править ]
Когда чужеродный патоген попадает в организм, специфические клетки, называемые антигенпрезентирующими клетками (APC), поглощают патоген посредством процесса, называемого фагоцитозом . Белки патогена перевариваются на небольшие кусочки ( пептиды ) и загружаются на антигены HLA (а именно, MHC класса II ). Затем они отображаются с помощью антиген-представляющих клеток на CD4 + Т - хелперов , [6] , которые затем производят различные эффекты и клетки к клетке , чтобы устранить взаимодействие патогена.
Посредством аналогичного процесса белки (как естественные, так и чужеродные, такие как белки вируса), продуцируемые внутри большинства клеток, отображаются на HLA (точнее, MHC класса I ) на поверхности клетки. Зараженные клетки могут распознаваться и разрушаться CD8 + Т-клетками . [6]
На изображении сбоку показан кусок ядовитого бактериального белка (пептид SEI), связанный внутри связывающей щели молекулы HLA-DR1. На иллюстрации далеко ниже, другой вид, можно увидеть весь DQ со связанным пептидом в аналогичной щели, если смотреть сбоку. Пептиды, связанные с заболеваниями, помещаются в эти «прорези», как рука в перчатке. Связанные пептиды представляются Т-клеткам. Т-клетки требуют презентации через молекулы MHC для распознавания чужеродных антигенов - требование, известное как ограничение MHC.. Т-клетки имеют рецепторы, подобные рецепторам В-клеток, и каждая Т-клетка распознает только несколько комбинаций пептидов класса II MHC. Как только Т-клетка распознает пептид в молекуле МНС класса II, она может стимулировать В-клетки, которые также распознают ту же молекулу в своих В-клеточных рецепторах. Таким образом, Т-клетки помогают В-клеткам вырабатывать антитела к тем же чужеродным антигенам. Каждый HLA может связывать множество пептидов, и каждый человек имеет 3 типа HLA и может иметь 4 изоформы DP, 4 изоформы DQ и 4 изоформы DR (2 из DRB1 и 2 из DRB3, DRB4 или DRB5), всего 12 изоформ. В таких гетерозиготах белкам, связанным с заболеванием, трудно избежать обнаружения.
При отторжении трансплантата [ править ]
Любая клетка, демонстрирующая какой-либо другой тип HLA, является «чужой» и рассматривается иммунной системой организма как захватчик, что приводит к отторжению ткани, несущей эти клетки. Это особенно важно в случае пересаженной ткани, поскольку это может привести к отторжению трансплантата . Из-за важности HLA для трансплантации локусы HLA являются одними из наиболее часто типируемых с помощью серологии и ПЦР. Было показано, что типирование HLA с высоким разрешением (HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1 и HLA-DPB1) может иметь значение при трансплантации для определения полного соответствия, даже если донор связанные с. [7]
| Аллель HLA | Заболевания с повышенным риском | Относительный риск |
|---|---|---|
| HLA-B27 | Анкилозирующий спондилоартрит | 12 [8] |
| Реактивный артрит | 14 [8] | |
| Острый передний увеит | 15 [8] | |
| HLA-B47 | Дефицит 21-гидроксилазы | 15 [8] |
| HLA-DR2 | Системная красная волчанка | От 2 до 3 [9] |
| HLA-DR3 | Аутоиммунный гепатит | 14 [8] |
| Первичный синдром Шегрена | 10 [8] | |
| Сахарный диабет 1 типа | 5 [8] | |
| Системная красная волчанка | От 2 до 3 [9] | |
| HLA-DR4 | Ревматоидный артрит | 4 [8] |
| Сахарный диабет 1 типа | 6 [8] | |
| HLA-DR3 и -DR4 вместе | Сахарный диабет 1 типа | 15 [8] |
| HLA-DQ2 и HLA-DQ8 | Глютеновая болезнь | 7 [10] |
При аутоиммунитете [ править ]
Типы HLA передаются по наследству, а некоторые из них связаны с аутоиммунными нарушениями и другими заболеваниями. Люди с определенными антигенами HLA более склонны к развитию определенных аутоиммунных заболеваний, таких как диабет I типа , анкилозирующий спондилит , ревматоидный артрит , [11] целиакия , СКВ (системная красная волчанка), миастения гравис , миозит с тельцами включения , синдром Шегрена и т. Д. нарколепсия . [12]Типирование HLA привело к некоторому улучшению и ускорению диагностики целиакии и диабета 1 типа; однако, чтобы типизация DQ2 была полезной, требуется либо типирование с высоким разрешением B1 * (разрешение * 02: 01 из * 02: 02), типирование DQA1 *, либо серотипирование DR . Текущее серотипирование может решить, за один шаг, DQ8. HLA-типирование при аутоиммунных заболеваниях все чаще используется в качестве инструмента диагностики. При целиакии это единственный эффективный способ отличить родственников первой степени родства, находящихся в группе риска, от родственников, не входящих в группу риска, до появления иногда необратимых симптомов, таких как аллергия и вторичное аутоиммунное заболевание.
В раке [ править ]
Некоторые HLA-опосредованные заболевания непосредственно участвуют в развитии рака. Глютен-чувствительная энтеропатия связана с повышенным распространением Т-клеточной лимфомы, связанной с энтеропатией, а гомозиготы DR3-DQ2 относятся к группе самого высокого риска, с почти 80% случаев Т-клеточной лимфомы, связанной с глютен-чувствительной энтеропатией. Однако чаще молекулы HLA играют защитную роль, распознавая увеличение антигенов, которые не переносятся из-за низких уровней в нормальном состоянии. Аномальные клетки могут быть мишенью для апоптоза, который, как считается, опосредует многие виды рака до постановки диагноза.
При выборе партнера [ править ]
Есть свидетельства неслучайного выбора партнера по определенным генетическим характеристикам. [13] [14] Это привело к появлению области, известной как генетический подбор партнеров .
Классификация [ править ]
Белки MHC класса I образуют функциональный рецептор на большинстве ядерных клеток организма. [15]
В HLA имеется 3 основных и 3 минорных гена MHC класса I.
Major MHC класса I
- HLA-A
- HLA-B
- HLA-C
Минорные гены - это HLA-E , HLA-F и HLA-G . β 2 -микроглобулин связывается с субъединицами основного и второстепенного гена с образованием гетеродимера.
HLA кодирует 3 основных и 2 минорных белка MHC класса II . Гены класса II объединяются с образованием гетеродимерных (αβ) белковых рецепторов, которые обычно экспрессируются на поверхности антигенпрезентирующих клеток .
Основные белки МНС класса II встречаются только на антигенпрезентирующих клетках , В-клетках и Т-клетках . [15]
- HLA-DP
- α- цепь, кодируемая локусом HLA-DPA1
- β -цепь , кодируемые HLA - DPB1 локус
- HLA-DQ
- α- цепь, кодируемая локусом HLA- DQA1
- β- цепь, кодируемая локусом HLA- DQB1
- HLA-DR
- α- цепь, кодируемая локусом HLA- DRA
- 4 & beta; цепи (только 3 можно на человека), кодируемые HLA - DRB1 , DRB3 , DRB4 , DRB5 локусов
Другие белки MHC класса II, DM и DO, используются во внутреннем процессинге антигенов, нагружая антигенные пептиды, полученные из патогенов, на молекулы HLA антигенпрезентирующей клетки .
Номенклатура [ править ]
Современные аллели HLA обычно отмечаются с разной степенью детализации. Большинство обозначений начинаются с HLA- и имени локуса, затем * и некоторого (четного) количества цифр, обозначающих аллель. Первые две цифры указывают группу аллелей, также известных как супертипы. Старые методики типирования часто не могли полностью различить аллели, и поэтому останавливались на этом уровне. Цифры с третьей по четвертую указывают несинонимичный аллель. Цифры с пятой по шестую обозначают любые синонимичные мутации в кодирующей структуре гена. Седьмая и восьмая цифры различают мутации вне кодирующей области. Буквы, такие как L, N, Q или S, могут следовать за обозначением аллеля, чтобы указать уровень экспрессии или другие известные о нем негеномные данные. Таким образом, полностью описанный аллель может иметь длину до 9 цифр,не включая префикс HLA и обозначение локуса.[16]
Изменчивость [ править ]
Локусы MHC являются одними из наиболее генетически изменчивых кодирующих локусов у млекопитающих, и локусы HLA человека не являются исключением. Несмотря на то, что человеческая популяция несколько раз за свою историю проходила через сжатие, которое было способно фиксировать многие локусы, локусы HLA, по-видимому, пережили такое сжатие с большим количеством вариаций. [17] Из 9 локусов, упомянутых выше, большинство сохранило дюжину или более аллельных групп для каждого локуса, что является гораздо более сохраненной вариативностью, чем подавляющее большинство локусов человека. Это соответствует гетерозиготному или сбалансированному отбору.коэффициент для этих локусов. Кроме того, некоторые локусы HLA являются одними из самых быстро развивающихся кодирующих областей в геноме человека. Один механизм диверсификации был отмечен в исследовании племен Амазонки в Южной Америке, которые, по-видимому, претерпели интенсивную конверсию генов между вариабельными аллелями и локусами в пределах каждого класса генов HLA. [18] Реже отмечались продуктивные рекомбинации с более длинным радиусом действия через гены HLA, приводящие к образованию химерных генов.
Шесть локусов содержат более 100 аллелей, обнаруженных в человеческой популяции. Из них наиболее вариабельными являются HLA B и HLA DRB1. По состоянию на 2012 год количество определенных аллелей приведено в таблице ниже. Чтобы интерпретировать эту таблицу, необходимо учитывать, что аллель является вариантом нуклеотидной (ДНК) последовательности в локусе, так что каждый аллель отличается от всех других аллелей по крайней мере в одном положении (однонуклеотидный полиморфизм, SNP). Большинство этих изменений приводят к изменению аминокислотных последовательностей, что приводит к функциональным различиям белка от незначительных до значительных.
Есть проблемы, которые ограничивают это изменение. Некоторые аллели, такие как DQA1 * 05: 01 и DQA1 * 05: 05, кодируют белки с идентично обработанными продуктами. Другие аллели, такие как DQB1 * 0201 и DQB1 * 0202, продуцируют белки, которые функционально подобны. Для класса II (DR, DP и DQ) варианты аминокислот в пептид-связывающей щели рецептора имеют тенденцию продуцировать молекулы с различной связывающей способностью.
Тем не менее, частота генов наиболее распространенных аллелей (> 5%) HLA-A, -B, -C и HLA-DPA1, -DPB1, -DQA1, -DQB1 и -DRB1 из Южной Америки была получена из Южной Америки. типирование и секвенирование, проведенные в исследованиях генетического разнообразия, а также в случаях и в контролях. [19] Кроме того, была собрана информация о частотах аллелей генов HLA-I и HLA-II для европейской популяции. [20] [21] В обоих случаях распределение частот аллелей выявляет региональные вариации, связанные с историей популяций.
Таблицы вариантных аллелей [ править ]
Количество вариантных аллелей в локусах класса I согласно базе данных IMGT-HLA, последнее обновление - октябрь 2018 г .:
| MHC класс I | |
|---|---|
| локус | # [22] [23] |
| Основные антигены | |
| HLA A | 4340 |
| HLA B | 5 212 |
| HLA C | 3 930 |
| Минорные антигены | |
| HLA E | 27 |
| HLA F | 31 год |
| HLA G | 61 |
Количество вариантных аллелей в локусах класса II (DM, DO, DP, DQ и DR):
| MHC класс II | ||||
|---|---|---|---|---|
| HLA | - А1 | - B1 | От -B3 до -B5 1 | Теор. возможный |
| локус | # [23] | # [23] | # [23] | комбинации |
| DM- | 7 | 13 | 91 | |
| ДЕЛАТЬ- | 12 | 13 | 156 | |
| DP- | 67 | 1,014 | 16 036 | |
| DQ- | 95 | 1,257 | 34 528 | |
| DR- | 7 | 2,593 | 312 | 11 431 |
| 1 DRB3, DRB4, DRB5 имеют вариабельное присутствие у людей | ||||
Тип варианта элемента последовательности (SFVT) [ править ]
Большая степень вариабельности генов HLA создает серьезные проблемы при исследовании роли генетических вариаций HLA в заболеваниях. Исследования ассоциации с заболеванием обычно рассматривают каждый аллель HLA как единое целое, которое не освещает части молекулы, связанные с заболеванием. Karp DR et al. описывает новый подход к типу вариантов последовательностей (SFVT) для генетического анализа HLA, который классифицирует белки HLA на биологически значимые более мелкие признаки последовательности (SF) и их вариантные типы (VT). [24]Характеристики последовательности представляют собой комбинации аминокислотных сайтов, определенных на основе структурной информации (например, бета-лист 1), функциональной информации (например, связывание пептидного антигена) и полиморфизма. Эти элементы последовательности могут быть перекрывающимися, непрерывными или прерывистыми в линейной последовательности. Типы вариантов для каждого признака последовательности определяются на основе всех известных полиморфизмов в описываемом локусе HLA. Разделение HLA на категории SFVT применяется в анализе генетических ассоциаций, чтобы можно было идентифицировать эффекты и роли эпитопов, общих для нескольких аллелей HLA. Характеристики последовательностей и типы их вариантов описаны для всех классических белков HLA; международный репозиторий HLA SFVT будет поддерживаться в базе данных IMGT / HLA. [25] Инструмент для преобразования аллелей HLA в составляющие их SFVT можно найти на веб-сайте портала базы данных и анализа иммунологии (ImmPort). [26]
Общие, хорошо задокументированные и редкие аллели [ править ]
Хотя количество отдельных аллелей HLA, которые были идентифицированы, велико, приблизительно 40% этих аллелей кажутся уникальными, будучи идентифицированными только у отдельных людей. [27] [28] Примерно о трети аллелей сообщалось более трех раз у неродственных людей. [28] [29] Из-за этой вариации в скорости обнаружения отдельных аллелей HLA были предприняты попытки категоризировать аллели в каждом экспрессируемом локусе HLA с точки зрения их распространенности. Результатом является каталог общих и хорошо задокументированных (CWD) аллелей HLA [29] [30], а также каталог редких и очень редких аллелей HLA. [27] [28]
Общие аллели HLA определяются как наблюдаемые с частотой не менее 0,001 в контрольных популяциях не менее 1500 человек. [29] [30] Хорошо задокументированные аллели HLA изначально были определены как обнаруженные не менее трех раз у неродственных лиц [29], а теперь определяются как обнаруженные не менее пяти раз у неродственных лиц посредством применения последовательности метод типирования (SBT), или, по крайней мере, три раза с помощью метода SBT и в конкретном гаплотипе у неродственных людей. [30] Редкие аллели определяются как аллели, о которых сообщалось от одного до четырех раз, а очень редкие аллели - как те, о которых сообщалось только один раз. [27] [28]
Таблица аллелей HLA в каждой категории распространенности [ править ]
Хотя в настоящее время ВПЦ и редкие или очень редкие обозначения были разработаны с использованием различных наборов данных и различных версий базы данных IMGT / HLA , [28] [30] приблизительная доля аллелей в каждом локусе HLA в каждой категории, показан ниже.
| HLA Локус | Количество общих аллелей [30] | % общих аллелей [30] | Нет хорошо задокументированных аллелей [30] | % хорошо задокументированных аллелей [30] | № редких аллелей [28] | % редких аллелей [28] | № очень редких аллелей [28] | % очень редких аллелей [28] | % категоризированных аллелей |
|---|---|---|---|---|---|---|---|---|---|
| А | 68 | 3,4% | 178 | 8,8% | 145 | 21,5% | 280 | 41,6% | ~ 75% |
| B | 125 | 4,8% | 242 | 9,3% | 190 | 17,6% | 468 | 43,5% | ~ 75% |
| C | 44 | 2,8% | 102 | 6,6% | 77 | 21,4% | 154 | 42,8% | ~ 74% |
| DRB1 | 79 | 6,8% | 147 | 12,7% | 133 | 22,7% | 206 | 35,2% | ~ 77% |
| DRB3 | 5 | 8,6% | 7 | 12,1% | ~ 21% | ||||
| DRB4 | 6 | 40,0% | 2 | 13,3% | ~ 53% | ||||
| DRB5 | 5 | 25,0% | 3 | 15,0% | ~ 40% | ||||
| DQA1 | 15 | 31,9% | 4 | 8,5% | 9 | 26,5% | 7 | 20,6% | ~ 88% |
| DQB1 | 22 | 12,5% | 8 | 4,5% | 26 | 28,9% | 42 | 45,2% | ~ 91% |
| DPA1 | 6 | 17,6% | 0 | 0,0% | 4 | 14,8% | 15 | 55,6% | ~ 88% |
| DPB1 | 40 | 28,8% | 14 | 9,0% | 29 | 22,7% | 29 | 32,8% | ~ 90% |
| Все места | 415 | 5,3% | 707 | 9,0% | 613 | 20,6% | 1214 | 40,8% | ~ 76% |
Изучение типов HLA [ править ]
Названия серотипов и аллелей [ править ]
К HLA применяются две параллельные системы номенклатуры. Первая и самая старая система основана на серологическом (на основе антител) распознавании. В этой системе антигенам в конечном итоге были присвоены буквы и цифры (например, HLA-B27 или, сокращенно, B27). Была разработана параллельная система, которая позволила более точно определять аллели. В этой системе «HLA» используется в сочетании с буквой * и числом из четырех или более цифр (например, HLA-B * 08: 01, A * 68: 01, A * 24: 02 : 01N N = Null) для обозначения определенного аллеля в данном локусе HLA . Локусы HLA могут быть далее классифицированы на MHC класса I и MHC класса II.(или редко, локус D). Каждые два года составляется номенклатура, чтобы помочь исследователям интерпретировать серотипы в аллели. [22]
Серотипирование [ править ]
Для создания реагента для типирования берется кровь животных или людей, клетки крови отделяются от сыворотки, а сыворотка разбавляется до оптимальной чувствительности и используется для типирования клеток других людей или животных. Таким образом, серотипирование стало способом грубой идентификации рецепторов HLA и изоформ рецепторов. С годами антитела для серотипирования стали более совершенными, поскольку методы повышения чувствительности улучшились, и продолжают появляться новые антитела для серотипирования. Одна из целей серотипического анализа - заполнить пробелы в анализе. Можно предсказать на основе метода «квадратного корня», метода «максимального правдоподобия» или анализа семейных гаплотипов, чтобы учесть адекватно типизированные аллели. Эти исследования с использованием методов серотипирования часто выявляли:в частности, для неевропейского или северо-восточного азиатского населения много нулевых или пустых серотипов. Это было особенно проблематично для локуса Cw до недавнего времени, и почти половина серотипов Cw оказалась нетипизированной в обзоре человеческой популяции в 1991 году.
Есть несколько типов серотипов. Широкий серотип антигена - это грубая мера идентичности клеток. Например, серотип HLA A9 распознает клетки людей, несущих A23 и A24. Он также может распознавать ячейки, которые пропускаются A23 и A24 из-за небольших изменений. А23 и А24 являются расщепленными антигенами, но антитела, специфичные к любому из них, обычно используются чаще, чем антитела к широким антигенам.
Сотовый набор [ править ]
Типичным клеточным анализом является смешанная культура лимфоцитов (MLC), который используется для определения типов HLA класса II. [31] Клеточный анализ более чувствителен к выявлению различий HLA, чем серотипирование. Это связано с тем, что незначительные различия, не распознаваемые аллоантисерами, могут стимулировать Т-клетки. Эта типизация обозначается как типы Dw. Серотипированный DR1 клеточно определен как Dw1 или Dw20 и так далее для других серотипированных DR. В таблице [32] показаны связанные клеточные специфичности для аллелей DR. Тем не менее, клеточное типирование имеет несогласованность в реакции между индивидуумами клеточного типа, что иногда дает результаты, отличные от предсказанных. Наряду со сложностью клеточного анализа при создании и поддержании реагентов для клеточного типирования, клеточный анализ заменяется методом типирования на основе ДНК.[31]
Секвенирование генов [ править ]
Незначительные реакции на субрегионы, которые проявляют сходство с другими типами, могут наблюдаться на генные продукты аллелей группы серотипов. Последовательность антигенов определяет реактивность антител, и поэтому наличие хорошей способности к секвенированию (или типированию на основе последовательностей) устраняет необходимость в серологических реакциях. Следовательно, различные реакции серотипа могут указывать на необходимость секвенирования HLA человека для определения новой последовательности гена.
Широкие типы антигенов по-прежнему полезны, например, для типирования очень разнообразных популяций со многими неидентифицированными аллелями HLA (Африка, Аравия, [33] Юго-Восточный Иран [34] и Пакистан, Индия [35] ). Африка, Южный Иран и Аравия демонстрируют трудности с типизацией ранее заселенных территорий. Разнообразие аллелей делает необходимым использование широкого типирования антигенов с последующим секвенированием генов, поскольку существует повышенный риск ошибочной идентификации с помощью методов серотипирования.
В конце концов, семинар, основанный на последовательности, решает, какой новый аллель входит в какую серогруппу, либо по последовательности, либо по реактивности. После проверки последовательности ей присваивается номер. Например, новый аллель B44 может получить серотип (то есть B44) и идентификатор аллеля, то есть B * 44: 65, поскольку это 65-й обнаруженный аллель B44. Marsh et al. (2005) [22] можно рассматривать как кодовую книгу для серотипов и генотипов HLA, а также новую книгу, выходящую раз в два года с ежемесячными обновлениями в тканевых антигенах .
Фенотипирование [ править ]
Типирование генов отличается от секвенирования и серотипирования генов. В этой стратегии используются праймеры для ПЦР, специфичные для вариантной области ДНК (так называемая SSP-PCR ). Если продукт подходящего размера найден, предполагается, что аллель HLA идентифицирован. Последовательности новых генов часто приводят к усилению двусмысленности. Поскольку типирование генов основано на SSP-PCR, возможно, что новые варианты, в частности, в локусах класса I и DRB1, могут быть пропущены.
Например, SSP-PCR в клинической ситуации часто используется для идентификации фенотипов HLA. Примером расширенного фенотипа человека может быть:
A * 01: 01 / * 03: 01 , C * 07: 01 / * 07: 02 , B * 07: 02 / * 08: 01 , DRB1 * 03: 01 / * 15: 01 , DQA1 * 05: 01 / * 01: 02 , DQB1 * 02: 01 / * 06: 02
В целом это идентично расширенному серотипу: A1, A3, B7, B8, DR3, DR15 (2), DQ2, DQ6 (1).
Для многих популяций, таких как японцы или европейцы, типизировано так много пациентов, что новые аллели относительно редки, и, таким образом, SSP-PCR более чем достаточен для разрешения аллелей. Гаплотипы могут быть получены путем типирования членов семьи в тех регионах мира, где SSP-PCR не может распознать аллели, а типирование требует секвенирования новых аллелей. Области мира, где SSP-PCR или серотипирование могут быть неадекватными, включают Центральную Африку, Восточную Африку, части южной Африки, Аравию, Южный Иран, Пакистан и Индию.
Гаплотипы [ править ]
Гаплотип HLA представляет собой серию «генов» HLA (локусов-аллелей) по хромосоме, один передается от матери, а другой - от отца.
Приведенный выше фенотип является одним из наиболее распространенных в Ирландии и является результатом двух общих генетических гаплотипов :
А * 01: 01 ; С * 07: 01 ; В * 08: 01 ; DRB1 * 03: 01 ; DQA1 * 05: 01 ; DQB1 * 02: 01 (по серотипированию A1-Cw7-B8-DR3-DQ2 )
который называется «супер B8» или «предковый гаплотип» и
А * 03: 01 ; С * 07: 02 ; В * 07: 02 ; DRB1 * 15: 01 ; DQA1 * 01: 02 ; DQB1 * 06: 02 (путем серотипирования A3-Cw7-B7-DR15-DQ6 или более старой версии "A3-B7-DR2-DQ1")
Эти гаплотипы можно использовать для отслеживания миграций в человеческой популяции, потому что они часто очень похожи на отпечатки пальцев события, произошедшего в процессе эволюции. Гаплотип Super-B8 обогащен западными ирландцами, снижается по мере удаления от этого региона и встречается только в тех регионах мира, куда мигрировали западные европейцы. «A3-B7-DR2-DQ1» более широко распространен от Восточной Азии до Иберии. Гаплотип Super-B8 связан с рядом аутоиммунных заболеваний, связанных с диетой. Существует 100 000 расширенных гаплотипов, но лишь немногие из них демонстрируют видимый и узловой характер в человеческой популяции.
Роль аллельной вариации [ править ]
Исследования людей и животных предполагают гетерозиготный механизм отбора, действующий на эти локусы, как объяснение этой изменчивости. [36] Одним из предложенных механизмов является половой отбор, при котором самки могут обнаруживать самцов с разными HLA относительно их собственного типа. [37] Хотя локусы, кодирующие DQ и DP, имеют меньше аллелей, комбинации A1: B1 могут давать теоретический потенциал 7,755 гетеродимеров DQ и 5,270 DP αβ соответственно. Хотя в человеческой популяции и близко не существует такого количества изоформ, каждый человек может нести 4 вариабельные изоформы DQ и DP, увеличивая потенциальное количество антигенов, которые эти рецепторы могут представлять иммунной системе.
Исследования вариабельных положений DP, DR и DQ показывают, что остатки, контактирующие с пептидным антигеном, в молекулах класса II наиболее часто являются местом изменения первичной структуры белка. Следовательно, за счет комбинации интенсивных аллельных вариаций и / или спаривания субъединиц пептидные рецепторы класса II способны связывать почти бесконечные вариации пептидов длиной 9 или более аминокислот, защищая скрещиваемые субпопуляции от возникающих или эпидемических заболеваний. Люди в популяции часто имеют разные гаплотипы, и это приводит к множеству комбинаций, даже в небольших группах. Это разнообразие увеличивает выживаемость таких групп и препятствует эволюции эпитопов в патогенах, которые в противном случае могли бы быть защищены от иммунной системы.
Антитела [ править ]
HLA-антитела обычно не встречаются в природе и, за некоторыми исключениями, образуются в результате иммунологического заражения чужеродным материалом, содержащим чужеродные HLA, при переливании крови, беременности (отцовские антигены) или трансплантации органов или тканей.
Антитела против связанных с заболеванием гаплотипов HLA были предложены для лечения тяжелых аутоиммунных заболеваний. [38]
Было обнаружено, что донор-специфические HLA-антитела связаны с недостаточностью трансплантата при трансплантации почек, сердца, легких и печени.
Соответствие HLA для больных братьев и сестер [ править ]
При некоторых заболеваниях, требующих трансплантации гемопоэтических стволовых клеток , преимплантационная генетическая диагностика может быть использована для рождения брата или сестры с соответствующим HLA, хотя есть этические соображения. [39]
См. Также [ править ]
- HCP5
- Список аллелей лейкоцитарного антигена человека, связанных с кожными заболеваниями
Ссылки [ править ]
- ^ Ссылка, Genetics Home. «Комплекс гистосовместимости» . Домашний справочник по генетике . Дата обращения 1 мая 2020 .
- ↑ Matsumura M, Fremont DH, Peterson PA, Wilson IA (август 1992). «Новые принципы распознавания пептидных антигенов молекулами MHC класса I». Наука . 257 (5072): 927–34. Bibcode : 1992Sci ... 257..927M . DOI : 10.1126 / science.1323878 . PMID 1323878 .
- ^ Берроуз SR, Rossjohn J, Маккласки J (январь 2006). «Неужели мы слишком ограничились в картировании эпитопов CTL?». Trends Immunol . 27 (1): 11–6. DOI : 10.1016 / j.it.2005.11.001 . PMID 16297661 .
- ^ Гэлбрейт В., Вагнер М.С., Чао Дж., Абаза М., Эрнст Л.А., Недерлоф М.А. и др. (1991). «Визуализирующая цитометрия по многопараметрической флуоресценции». Цитометрия . 12 (7): 579–96. DOI : 10.1002 / cyto.990120702 . PMID 1782829 .
- Перейти ↑ Brennan PA, Kendrick KM (декабрь 2006 г.). «Социальные запахи млекопитающих: привлекательность и индивидуальное признание» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 361 (1476): 2061–78. DOI : 10.1098 / rstb.2006.1931 . PMC 1764843 . PMID 17118924 .
- ^ a b Тейлор CJ, Болтон EM, Брэдли JA (2011). «Иммунологические соображения для эмбриональных и индуцированных банков плюрипотентных стволовых клеток» . Философские труды Королевского общества B . 366 (1575): 2312–2322. DOI : 10,1098 / rstb.2011.0030 . PMC 3130422 . PMID 21727137 .
- ↑ Агарвал, Раджат Кумар; Кумари, Анкита; Седай, Амит; Пармар, Лалит; Дханья, Ракеш; Фолкнер, Лоуренс (2017). «Случай для типирования HLA с расширенными 6-локусами с высоким разрешением для выявления родственных доноров на Индийском субконтиненте» . Биология трансплантации крови и костного мозга . 23 (9): 1592–1596. DOI : 10.1016 / j.bbmt.2017.05.030 . PMID 28603069 .
- ^ a b c d e f g h i j Таблица 5-7 в: Mitchell, Richard Sheppard; Кумар, Винай; Аббас, Абул К .; Фаусто, Нельсон (2007). Базовая патология Роббинса . Филадельфия: Сондерс. ISBN 978-1-4160-2973-1. 8-е издание.
- ^ a b Значения даны для кавказцев согласно стр. 61 (правый столбец) в: Jane Salmon; Уоллес, Дэниел Дж .; Дюбуа, Эдмунд Л .; Kirou, Kyriakos A .; Хан, Бевра; Леман, Томас А. (2007). Красная волчанка Дюбуа . Филадельфия: Липпинкотт Уильямс и Уилкинс. ISBN 978-0-7817-9394-0.
- ^ Маргарит-Жаннин П., Баброн М.С., Бурджи М., Лука А.С., Сгусток F, Перкопо С., Кото I, Хьюго Дж. П., Ашер Н., Соллид Л. М., Греко Л., Клерже-Дарпу F (июнь 2004 г.). «Относительные риски HLA-DQ для целиакии в европейских популяциях: исследование Европейского генетического кластера по целиакии». Тканевые антигены . 63 (6): 562–7. DOI : 10.1111 / j.0001-2815.2004.00237.x . PMID 15140032 .
- ^ Kurkó Дж, Besenyei Т, J Laki, Glant ТТ, Mikecz К, Szekanecz Z (2013). «Генетика ревматоидного артрита - всесторонний обзор» . Clin Rev Allergy Immunol . 45 (2): 170–9. DOI : 10.1007 / s12016-012-8346-7 . PMC 3655138 . PMID 23288628 .
- ^ Миньо, Эммануэль; Линь, Линг; Роджерс, Уильям; Хонда, Ютака; Цю, Сяохун; Линь, Сяоянь; Окунь, Микеле; Ходжох, Хирохико; Мики, Тетсуро; Hsu, Susan H; Леффелл, Мэри S; Грумет, Ф. Карл; Фернандес-Вина, Марсело; Хонда, Макото; Риш, Нил (2001). «Сложные взаимодействия HLA-DR и -DQ создают риск нарколепсии-катаплексии в трех этнических группах» . Американский журнал генетики человека . 68 (3): 686–699. DOI : 10.1086 / 318799 . PMC 1274481 . PMID 11179016 .
- ^ Jokiniemi, А., Magris, М., Ritari J., Kuusipalo, Л., Лундгрен, Т., Partanen J., Kekäläinen, J. Пост-совокупительный генетическая сватовства: HLA-зависимые эффекты цервикальной слизи на человека функция спермы. Труды Королевского общества B (2020). http://dx.doi.org/10.1098/rspb.2020.1682
- ^ Jokiniemi, A., Kuusipalo, L., Ritari, J., Koskela, S., Partanen, J., Kekäläinen, J. Иммуногенетическая несовместимость на уровне гамет у людей - к более глубокому пониманию оплодотворения и бесплодия? Наследственность (2020). https://doi.org/10.1038/s41437-020-0350-8
- ^ а б Чу SY (2008). «Система HLA: генетика, иммунология, клинические испытания и клиническое значение» . Йонсей Медицинский журнал . 48 (1): 11–23. DOI : 10.3349 / ymj.2007.48.1.11 . PMC 2628004 . PMID 17326240 .
- ^ "Номенклатура HLA @ hla.alleles.org" . hla.alleles.org . Архивировано 2 мая 2018 года . Дата обращения 2 мая 2018 .
- ^ Шеннан, Дуглас Х (2006). Эволюция и спираль технологий . Издательство Trafford Publishing. ISBN 978-1-55212-518-2.
- Перейти ↑ Parham P, Ohta T (апрель 1996). «Популяционная биология презентации антигена молекулами MHC класса I». Наука . 272 (5258): 67–74. Bibcode : 1996Sci ... 272 ... 67P . DOI : 10.1126 / science.272.5258.67 . PMID 8600539 . S2CID 22209086 . .
- ^ Рекена, Дэвид; Médico, Aldhair; Chacón, Ruy D .; Рамирес, Мануэль; Марин-Санчес, Оберт (2020). «Идентификация новых эпитопов-кандидатов на белках SARS-CoV-2 для Южной Америки: обзор частот HLA по странам» . Границы иммунологии . 11 : 2008. DOI : 10.3389 / fimmu.2020.02008 . ISSN 1664-3224 . PMC 7494848 . PMID 33013857 .
- ^ Нуньес, JM; Buhler, S .; Рёссли, Д .; Санчес-Мазас, А. (2014). «Программа HLA-net GENE [RATE] для эффективного анализа данных HLA и его применение к 145 выборкам населения из Европы и соседних регионов» . Тканевые антигены . 83 (5): 307–323. DOI : 10.1111 / tan.12356 . ISSN 1399-0039 . PMID 24738646 .
- ^ Санчес-Мазас, Алисия; Бюлер, Стефан; Нуньес, Хосе Мануэль (2013). «Новая HLA-карта Европы: региональные генетические вариации и их значение для анамнеза, исследования ассоциаций болезней и трансплантации тканей» . Человеческая наследственность . 76 (3–4): 162–177. DOI : 10.1159 / 000360855 . ISSN 0001-5652 . PMID 24861861 .
- ^ а б в Марш, SG; Альберт, ED; Бодмер, ВФ; Bontrop, RE; Dupont, B .; Эрлих, HA; Fernández-Viña, M .; Джерати, Делавэр; Holdsworth, R .; Херли, СК; Lau, M .; Ли, кВт; Мах, Б .; Maiers, M .; Mayr, WR; Мюллер, CR; Parham, P .; Петерсдорф, EW; Сасадзуки, Т .; Строминджер, JL; Svejgaard, A .; Терасаки, ИП; Tiercy, JM; Троусдейл, Дж. (2010). «Номенклатура факторов системы HLA, 2010» . Тканевые антигены . 75 (4): 291–455. DOI : 10.1111 / j.1399-0039.2010.01466.x . PMC 2848993 . PMID 20356336 .
- ^ a b c d Услуги, EBI Web. «Статистика <IMGT / HLA <IPD <EMBL-EBI» . www.ebi.ac.uk . Архивировано 20 сентября 2012 года . Дата обращения 2 мая 2018 .
- ↑ Karp DR, Marthandan N, Marsh SG, Ahn C, Arnett FC, Deluca DS, Diehl AD, Dunivin R, Eilbeck K, Feolo M, Guidry PA, Helmberg W., Lewis S, Mayes MD, Mungall C, Natale DA, Peters Б., Петерсдорф Э., Ревейл Д. Д., Смит Б., Томсон Г., Валлер М. Дж., Шойерманн Р. Х. (февраль 2010 г.). «Анализ новых вариантов последовательности признаков генетической ассоциации HLA при системном склерозе» . Молекулярная генетика человека . 19 (4): 707–19. DOI : 10,1093 / HMG / ddp521 . PMC 2807365 . PMID 19933168 .
- ^ «База данных IMGT / HLA» . Архивировано 24 сентября 2006 года.
- ^ "База данных иммунологии и аналитический портал (ImmPort)" . Архивировано из оригинального 26 июля 2011 года.
- ^ a b c Миддлтон Д., Гонсалес Ф., Фернандес-Вина М., Тирси Дж. М., Марш С. Г., Обри М., Бикальо М. Г., Каносси А., Картер В., Кейт С., Герини Ф. Р., Луазо П., Мартинетти М., Мораес М., Моралес В. , Перасаари Дж., Сеттерхольм М., Спраг М., Тавуларис С., Торрес М., Видал С., Витт С., Вольвенд Дж., Ян К. Л. (декабрь 2009 г.). «Биоинформатический подход к установлению редкости аллелей HLA». Тканевые антигены . 74 (6): 480–5. DOI : 10.1111 / j.1399-0039.2009.01361.x . PMID 19793314 .
- ^ a b c d e f g h i Гонсалес-Галарса Ф. Ф., Мак С. Дж., Холленбах Дж., Фернандес-Вина М., Сеттерхольм М., Кемпенич Дж., Марш С. Г., Джонс А. Р., Миддлтон Д. (февраль 2013 г.). «16 (th) IHIW: расширение количества ресурсов и биоинформатический анализ для исследования редких аллелей HLA». Международный журнал иммуногенетики . 40 (1): 60–5. DOI : 10.1111 / iji.12030 . PMID 23198982 . S2CID 205192491 .
- ^ a b c d Кано П., Клиц В., Мак SJ, Майерс М., Марш С. Г., Норин Х., Рид Э. Ф., Сеницер Д., Сеттерхольм М., Смит А., Фернандес-Винья М. (май 2007 г.). «Общие и хорошо задокументированные аллели HLA: отчет Специального комитета Американского общества гистосовместимости и иммуногенетики». Иммунология человека . 68 (5): 392–417. DOI : 10.1016 / j.humimm.2007.01.014 . PMID 17462507 .
- ^ a b c d e f g h Mack SJ, Cano P, Hollenbach JA, He J, Hurley CK, Middleton D, Moraes ME, Pereira SE, Kempenich JH, Reed EF, Setterholm M, Smith AG, Tilanus MG, Torres M , Varney MD, Voorter CE, Fischer GF, Fleischhauer K, Goodridge D, Klitz W., Little AM, Maiers M, Marsh SG, Müller CR, Noreen H, Rozemuller EH, Sanchez-Mazas A, Senitzer D, Trachtenberg E, Fernandez- Вина М (апрель 2013 г.). «Распространенные и хорошо задокументированные аллели HLA: обновление каталога CWD за 2012 год» . Тканевые антигены . 81 (4): 194–203. DOI : 10.1111 / tan.12093 . PMC 3634360 . PMID 23510415 .
- ^ а б Херли СК (1997). «Типирование HLA на основе ДНК для трансплантации». В Leffell MS, Donnenberg AD, Rose NR, eds. (1997) Справочник по иммунологии человека. С. 521–55, Бока-Ратон: CRC Press , ISBN 0-8493-0134-3 .
- ^ Bodmer JG, Marsh SG, Albert ED, Bodmer WF, Dupont B, Erlich HA и др. (Май 1992 г.). «Номенклатура факторов системы HLA, 1991». Иммунология человека . 34 (1): 4–18. DOI : 10.1016 / 0198-8859 (92) 90079-3 . PMID 1399721 .
- ^ Valluri В, Valluei В, Мустафа М, Santhosh А, Д Мидлтон, Алвариш М, Alvales М, Эль - Хадж Е, Gumama О, Abdel-Wareth л, Abdel-Waieth л (август 2005 г.). «Частоты фенотипов HLA-A, HLA-B, HLA-DR и HLA-DQ в популяции Объединенных Арабских Эмиратов». Тканевые антигены . 66 (2): 107–13. DOI : 10.1111 / j.1399-0039.2005.00441.x . PMID 16029430 .
- ^ Фарджадиан С, Нарус Т, Кавата Х, Гадери А, Бахрам С, Иноко Х (ноябрь 2004 г.). «Молекулярный анализ частот и гаплотипов HLA аллелей у белуджей Ирана по сравнению с родственными популяциями Пакистана». Тканевые антигены . 64 (5): 581–7. DOI : 10.1111 / j.1399-0039.2004.00302.x . PMID 15496201 .
- ^ Shankarkumar U, Prasanavar D, K Гош, Mohanty D (май 2003). «Частоты аллелей HLA A * 02 и ассоциации гаплотипов B у западных индейцев». Иммунология человека . 64 (5): 562–6. DOI : 10.1016 / S0198-8859 (03) 00032-6 . PMID 12691707 .
- ^ Apanius В, D Пенна, PR - Slev, Ruff Л.Р., Потс WK (1997). «Природа отбора по основному комплексу гистосовместимости». Критические обзоры в иммунологии . 17 (2): 179–224. DOI : 10,1615 / critrevimmunol.v17.i2.40 . PMID 9094452 . .
- ^ Ведекинд С, Т Зеебека, Bettens F, Paepke AJ (июнь 1995). «MHC-зависимые предпочтения спаривания у людей». Труды Королевского общества B: биологические науки . 260 (1359): 245–9. Bibcode : 1995RSPSB.260..245W . DOI : 10,1098 / rspb.1995.0087 . PMID 7630893 . S2CID 34971350 .
- ^ Осима M, Deitiker P, T Ashizawa, Atassi MZ (май 2002). «Вакцинация пептидом MHC класса II ослабляет клеточные и гуморальные ответы против tAChR и подавляет клинический EAMG». Аутоиммунитет . 35 (3): 183–90. DOI : 10.1080 / 08916930290022270 . PMID 12389643 . S2CID 5690960 .
- ^ Верлинский Y, Речицкий S, Скулкрафт Вт, Стром С, Кулиев А (июнь 2001 г.). «Преимплантационная диагностика анемии Фанкони в сочетании с HLA-сопоставлением» . JAMA . 285 (24): 3130–3. DOI : 10,1001 / jama.285.24.3130 . PMID 11427142 .
Библиография [ править ]
- Дэниел М. Дэвис, Ген совместимости , Лондон, Penguin Books , 2014 ( ISBN 978-0-241-95675-5 ).
- Жолт Харсани и Ричард Хаттон, Ричард, Генетическое пророчество: за пределами двойной спирали , Лондон: Гранада, 1982 ( ISBN 0-246-11760-5 ).
Внешние ссылки [ править ]
- База данных последовательностей IMGT / HLA в Европейском институте биоинформатики
- hla.alleles.org
- HLA Informatics Group в The Anthony Nolan Trust
- Британское общество гистосовместимости и иммуногенетики
- Американское общество гистосовместимости и иммуногенетики
- Европейская федерация иммуногенетики
- Инструмент HistoCheck HLA для трансплантации органов и стволовых клеток
- Частоты аллелей в переменных локусах, связанных с иммунитетом
- Человек + лейкоциты + антигены в предметных рубриках Национальной медицинской библиотеки США (MeSH)
- dbMHC Home, база данных NCBI по основному комплексу гистосовместимости
- Проект редких аллелей в базе данных AlleleFrequencies Net (AFND)
- Каталог общих и хорошо документированных (CWD) аллелей
